Fundamento General
La AAOT diseña su actividad académica con el propósito de proveer al profesional de conocimientos, destrezas y actitudes conducentes a la “calidad global del acto médico”.
Estatuto de la AAOT
TITULO IX
DE LOS DERECHOS DE LA ESPECIALIDAD Y DEL ESPECIALISTA
ARTICULO XLIX: La Asociación propiciará por todos los medios que estime convenientes la jerarquización de la especialidad ante las instituciones públicas y privadas del país.
ARTICULO L: Velará por el correcto ejercicio de la especialidad por parte de sus miembros desde el punto de vista de la ética y de la deontología, según reglamentaciones dictadas por ella misma a tal efecto, o que se dicten en el futuro. Propenderá a la obtención de un honorario ético y justo para los especialistas por medio de un Nomenclador de prácticas especializadas, en forma individual o mancomunada con otras instituciones o Asociaciones.
Definición
El Registro de Implantes (RI) es un Organo Colegiado de la AAOT
La asignación de responsabilidades de los integrantes del RI es específica.
Organización y funciones de sus integrantes:
– Presidente: Asume la responsabilidad de la gestión del RI.
En consenso con sus colegas integrantes del RI propone a la CD la visión estratégica y el plan de acción.
– Secretario Técnico: colabora en la elaboración de los proyectos; supervisa la progresión del proceso de gestión
– Asistente Administrativo: Aporta su conocimiento a la visión multidisciplinar y taxonómica propia del RI.
Su perfil se orienta a un profesional o técnico con formación en Metodología de la Investigación, Monitoreo de Ensayos Clínicos y/o Gestión de Procesos.
– Asesor Legal
– Asesor Informático
– Consultores técnicos en materias específicas: Cirugía reconstructiva del adulto, Trauma, Ortopedia Oncológica, Mano y Cirugía reconstructiva del Miembro superior, Ortopedia Infantil, Columna Vertebral, Artroscopía.
Misión
El RI cumple un rol específico como instrumento de registro con finalidad estadística.
Asimismo, el RI es un Agente de Tecnovigilancia.
– Agente de Tecnovigilancia. Según la definición de ANMAT: “…se entiende por Tecnovigilancia al conjunto de métodos y observaciones que permiten investigar eventos e incidentes adversos previos o posteriores a la utilización de un producto médico.”
El ANMAT ha creado el Programa de Tecnovigilancia (Disposición Nº 8054/10). Las funciones de dicho programa consisten en recoger, evaluar y organizar la información sobre los Eventos Adversos y fallas de calidad reportados durante la comercialización de los productos médicos.
Complétela y envíela a registro.secretaria@aaot.org.ar
Registro de Implantes
Asociación Argentina de Ortopedia y Traumatología
Tel: 4801-2320. Int. 261. L a V de 12 a 19 hs
e-mail: registro.secretaria@aaot.org.ar
Centros Centinela (CC)
Son centros asistenciales que asumen la responsabilidad de alimentar la Base de Datos del RI.
El “modus operandi” respetará la privacidad del paciente y del equipo médico tratante acorde con la legislación vigente.
Fase Inductoria:
En consenso con la CD de la AAOT se ha definido un período no menor de 6 (seis) meses y no mayor de 12 (doce) meses durante el cual se ajustarán los procesos inherentes a la recolección y procesamiento de datos.
Durante esta fase, la nómina de CC será limitada a una serie de centros que cumplen con las siguientes características:
A- Concentración de volumen de actividad
B- Capacidad de enrolamiento
C- Antecedentes de comunicar reportes verificables y confiables
Durante la Fase Inductoria se enrolarán los siguientes procedimientos:
1- Artroplastías
2- Osteosintesis
3- Artroscopía
4- Columna
Los CC deberán cumplir los siguientes requisitos fundamentales:
1- Veracidad
(Veraz: adj. Que dice, usa o profesa siempre la verdad. Fuente: www.rae.es)
2- Trazabilidad
(1. Posibilidad de identificar el origen y las diferentes etapas de un proceso de producción y distribución de bienes de consumo./ 2. Reflejo documental de estas etapas. Fuente: www.rae.es)
El RI preservará los datos aportados por los CC.
Dichos datos serán de utilización confidencial garantizando el secreto profesional y la identidad de las personas (Ley de Habeas data)
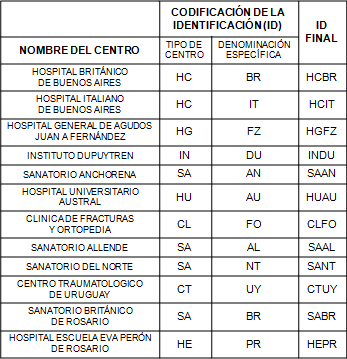
De acuerdo al Acta Nº 1012 de la Comisión Directiva de la AAOT del 26 de julio de 2011, los CC aprobados para la Etapa Inductoria del Registro de Implantes, son los siguientes:
Ciudad Autónoma de Buenos Aires:
Hospital Británico de Buenos Aires
Hospital Italiano de Buenos Aires
Hospital General de Agudos «Juan A. Fernández»
Instituto Dupuytren
Sanatorio Anchorena
Provincia de Buenos Aires:
Hospital Universitario Austral (Pilar)
Clínica de Fracturas y Ortopedia (Mar del Plata)
Provincia de Córdoba:
Sanatorio Allende
Provincia de Tucumán:
Sanatorio del Norte
Provincia de Entre Ríos:
Centro Traumatológico Uruguay
Provincia de Santa Fe:
Sanatorio Británico (Rosario)
Hospital Escuela Eva Perón (Rosario)
CENTROS CENTINELA
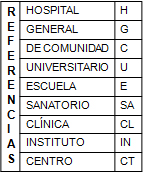
El Programa de Alerta Amarilla establecido dentro del Convenio Marco entre la AAOT y la ANMAT, le da la posibilidad al profesional de cumplir con la Notificación de Tecnovigilancia de una Falla o Desvío de la calidad, un Reporte de Evento Adverso o Evento Adverso Serio a la Dirección de Tecnovigilancia de la ANMAT a través de este Registro de Implantes.
Para facilitar la tarea de discernimiento entre los Eventos, facilitamos las definiciones empleadas para Producto Médico dentro del Mercosur (Entiéndase la terminología “utilización en el Mercosur” cuando un Producto Médico está en uso en por lo menos uno de los Estados Partes). Fuente: www.anmat.gov.ar
–Desvío de la calidad: Alejamiento de los parámetros de la calidad declarados por el fabricante, para un producto médico, en el momento de su registro ante la autoridad sanitaria competente.
–Evento Adverso: daño a la salud ocasionada a un usuario, paciente o a otra persona durante el uso de un producto médico.
–Evento Adverso Grave: Evento adverso que encaja en al menos una de las siguientes situaciones:
-
Conduce a la muerte;
-
Causa daños permanentes o deficiencia en una estructura del organismo;
-
Requiere intervención médica o quirúrgica a fin de prevenir el deterioro permanente de una función o estructura del cuerpo;
-
Requiere la hospitalización de paciente o la prolongación de la hospitalización;
-
Conduce a una interrupción o riesgo fetal, muerte fetal o anomalía congénita. (Referente a un Producto Médico a través del Registro de Implantes de la AAOT)
–Fabricante: persona que proyecta, fabrica, ensambla o procesa un producto terminado, incluyendo terceros proveedores autorizados para esterilizar, rotular y/o envasar.
–Notificación: comunicación de un evento adverso o desvío de la calidad, recibida por la autoridad sanitaria, relacionada con un producto médico.
Registro de Implantes AAOT
FUENTES DE INSPIRACIÓN
La fuente de inspiración han sido los principales Registros de Implantes reconocidos mundialmente
Certificado de habilitación y autorización de funcionamiento de la empresa
Certificado de Buenas Prácticas de Fabricación vigente
Listado de productos (familias)
Copia del Certificado de Registro de Producto








